Chemie voor beginners
In de letterlijke zin van het woord heet een stof die een chemische reactie bewerkstelligt, maar daarbij niet verbruikt wordt een "katalysator". Katalyse is de naam voor chemische processen waarbij een reactie tussen twee stoffen mogelijk wordt gemaakt door een derde stof (de katalysator), die zelf niet aan de reactie deelneemt. De reactie wordt mogelijk doordat de katalysator er via een ingewikkeld chemisch proces in slaagt om de binding tussen de atomen in de twee stoffen los te maken, zodat die een reactie met elkaar kunnen aangaan.
De makelaar
Eenvoudiger gesteld: je zou een katalysator kunnen vergelijken met een huwelijksmakelaar die twee mensen bij elkaar brengt, met als doel een huwelijk tussen beide partijen. In de chemie gaat dat ongeveer op dezelfde manier. De chemische makelaar (katalysator) brengt twee stoffen bij elkaar, met als doel het vormen van een nieuwe verbinding. Net als de huwelijksmakelaar niet na één succesvolle verbintenis is opgebruikt is de chemische variant dat ook niet: hij kan nog jarenlang vele mensen (moleculen) tot elkaar brengen.
Schadelijke stoffen
En dan komen we meteen aan bij het nut van de katalysator: het onschadelijk maken van schadelijke stoffen. Bij een verbrandingsmotor gaat het hoofdzakelijk om stikstofoxiden, koolstofmonoxiden (CO) en onverbrande koolwaterstoffen. In de uitlaatgassen van een verbrandingsmotor worden deze door de katalysator zo ver mogelijk omgezet in kooldioxide en water, terwijl een ander gedeelte met NOx reageert tot het onschuldige stikstofgas (N2).
De chemische reacties zien er als volgt uit:
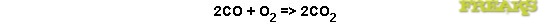
In het geval van het "potje" dat onder onze auto"s en motoren in de onmiddellijke nabijheid van de motor hangt bestaat de katalysator uit het materiaal platina, of een legering van platina en rhodium.
Tekst: Hans van Rijsse
De katalysator ontleed
De driewegkatalysator
Driewegkatalysatoren worden tegenwoordig alom toegepast om uitlaatgassen te ontdoen van schadelijke componenten. "Drieweg" slaat op het simultaan verlopen van drie reacties bij de katalysator:
- Oxidatie van in de motor niet verbrande koolwaterstoffen
- Oxidatie van door de motor geproduceerd koolmonoxide
- Reductie van geproduceerde stikstofoxiden
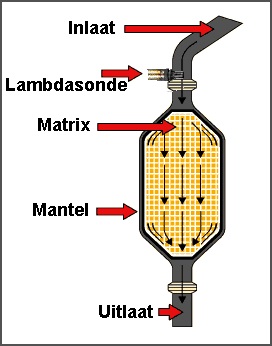
De driewegkatalysator zet deze stoffen om in kooldioxide, water, en stikstof. Om de oxidatie- en reductiereacties tegelijk te laten verlopen is het noodzakelijk om een chemisch ideaal (officiële benaming: stoichiometrisch) lucht/brand-stofmengsel aan de motor te voeden. Dit wordt gerealiseerd door precieze brandstof-injectie in de cilinders via een microprocessorregeling, die op zijn beurt wordt aangestuurd door de zogenaamde lambda-sonde. Deze lijkt wat op een bougie en word vlak voor de katalysator gemonteerd. Nu is ook duidelijk waarom het onmogelijk is om dit type katalysator te combineren met carburateurs: deze reageren niet alleen te traag, maar mengen brandstof en lucht ook te onnauwkeurig om van enig nut te zijn.
De Lambda-sonde
Een katalysator kan zijn werk alleen naar behoren doen als aan twee voorwaarden is voldaan: een werktemperatuur van 300 tot 400 graden Celsius en een brandstof-luchtmengsel dat dicht tegen de verhouding 1:14,7 ligt. De verhouding tussen brandstof en lucht noemt men Lambdawaarde, waarbij de verhouding 1:14,7 gelijk staat aan Lambdawaarde 1. De effectiviteit van de katalysator bij het omzetten van stikstofoxiden daalt scherp wanneer de Lambdawaarde boven de waarde 1 uitkomt, en is vrijwel nihil bij een waarde van 1,02 of hoger. De omzetting van CO (koolmonoxide) verloopt juist beter als omgezet naarmate de Lambdawaarde hoger wordt (armer brandstofmengsel).

Vandaar dat een katalysator slechts effectief kan worden toegepast wanneer het brandstof/luchtmengsel steeds op de ideale verhouding wordt gehouden met behulp van een lambda-sonde. Wanneer deze vóór de katalysator gemonteerde sonde ook maar een geringe afwijking van Lambda 1 vaststelt, dan zal het motormanagement het mengsel rijker of armer maken. Dit proces voltrekt zich continu en vele malen per seconde.





